由于CT具有的应用广泛,快速以及可重复性好等特点,它在许多病变的诊断中发挥着重要作用;然而,近年来人们对与辐射剂量有关的问题越来越重视,特别是对于需要定期CT随访的儿科或肿瘤患者。我们一直致力于采用新技术,在不影响诊断图像质量的前提下减少辐射剂量,遵守 “ALARA”原则。
为了克服这些缺点,CT供应商开发了自动管电压和管电流调制(参见XI区:自动管电流调制技术的原理和使用注意事项)技术,能够在不影响诊断准确性的情况下减少辐射剂量。图像重建技术对CT辐射剂量和图像质量有重大影响。在临床实践中,第一个用于图像重建的分析方法是滤波反投影(FBP),已经常规使用了几十年。FBP的主要优点是重建速度快和图像质量好,而主要缺点是在低剂量(LD)CT采集时图像质量下降,特别是在肥胖患者和有金属装置时。混合IR(HIR)算法包括一个单一的后向投影步骤,同时应用于原始数据和图像领域,以分别减少伪影和噪声。基于模型的IR(MBIR)算法包括后向重建步骤(其中图像由投影数据产生),以及前向重建步骤(包括从先前产生的图像中检索投影数据,从而产生人工数据,反过来与原始数据进行比较);最后在比较后应用IR噪声过滤算法。今天我们分享一篇文献,概述IR算法在临床上的应用,阐述其主要优势和局限性,并阐明AI新时代的未来前景。
01 技术特点
滤波反投影
为了更好理解迭代重建模式的基本要点,首先必须概述FBP的主要方面。滤波反投影(Filtered back-projection,FBP)是一种从投影数据(正弦图)中通过在进行反投影步骤之前应用高通滤波器(称为斜坡滤波器)来重建图像的解析算法。斜坡滤波器抑制了衰减轮廓的低空间频率成分,从而最终抑制模糊并增强边缘。然而,该滤波器增加了图像噪声,因此会导致斑点状图像外观。此外,可以将斜坡滤波器与不同强度的滤波器(卷积核)结合使用,从而增加最终图像的空间分辨率(不同的卷积核可以优化软组织或高对比结构的显示),但代价是更高的图像噪声。
FBP的优点包括稳定性和快速图像重建,还可以根据用户的具体需求提供定制的滤波器,有利于生成符合阅片习惯的噪声结构和纹理的输出图像。因为这些原因,FBP在过去的30年里代表了标准的CT图像重建算法,在标准辐射剂量下生成具有高诊断质量的图像。
辐射相关的健康风险的增加促使社会各界采取策略来降低CT辐射剂量。FBP的主要弱点涉及FBP本身的内在特点:图像的清晰度和噪声直接相关;因此,滤波步骤增强了低剂量CT数据中的图像噪声和伪影。事实上,以低辐射剂量获取并使用FBP重建的CT扫描图像会显著降低图像质量,包括噪声增加、低对比度可检测性差以及由于光子缺乏而产生的伪影(例如条纹状伪影)。因此,FBP在减少剂量方面的潜力微乎其微,而且有损诊断图像质量的风险;因此,它已被迭代重建算法所取代。
迭代重建
迭代重建技术可以在较低辐射剂量下进行CT扫描,同时减轻图像噪声,因此与相同条件下的FBP相比,可以获得更高的图像质量。早在20世纪70年代初就引入了第一个迭代重建算法,即代数重建;然而,由于CT重建工作站计算能力有限,这种技术从未真正起飞。几十年后,计算能力的提升使得IR技术在CT成像中得以引入。2009年,美国食品药品监督管理局批准了第一个IR算法IRIS(IR in image space; Siemens Healthineers, Erlangen, Germany),该算法使用单一的后向投影步骤,从原始数据创建截面图像。正如其名称所示,IR方法对图像重建进行多次迭代,以更好地评估数学假设,并将优化的数据与原始数据进行比较;每次迭代将图像更新为噪声较少的图像,最终导致优化的低噪声输出数据集。更多的迭代会导致更长的重建时间,尤其是对于在原始数据空间中也进行的混合迭代;因此,CT数据需要强大的计算能力和充足的重建时间。图1显示了CT数据通过FBP和IR算法进行重建的示意图。
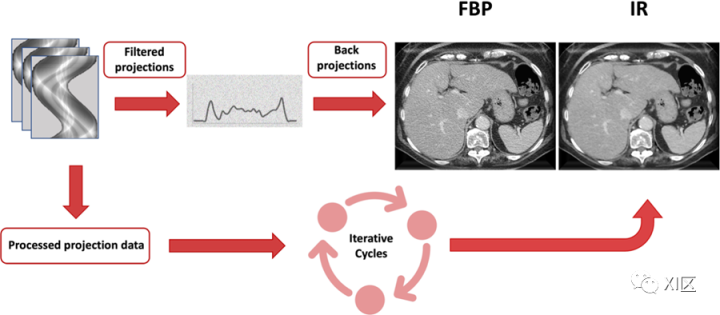
图1 CT数据重建的示意图。通过滤波反投影(FBP)和迭代重建(IR)算法重建CT数据的示意图。
迭代重建技术可以是混合型,也可以基于模型。混合型IR是一种通过迭代方法减少图像噪声的统计算法,而基于模型的IR算法考虑了采集过程、系统几何和图像统计。混合IR算法在初始和最终阶段分别对数据进行迭代滤波;此过程可以仅在投影空间或图像空间中进行,或两者都进行。在投影空间中,通过统计模型进行相邻投影数据的比较,以识别过于嘈杂的投影数据,从而使其变化最小化。
相反,基于模型的IR算法通过至少1次前向投影来模拟投影数据,并进行反向重建,重复固定次数或直到修正变得可以忽略为止;然后从投影数据重建图像,并从图像生成人工投影数据。因此,基于模型的IR需要模型或图像对象的估计来初始化迭代周期。与混合IR相比,基于模型的IR旨在明显减少图像噪声、改善低对比度细节和提高空间分辨率,与HIR相比,辐射剂量减少更高。然而,基于模型的IR需要非常高的计算能力,导致重建时间长,并且可能通过生成过度平滑的图像纹理来对图像质量产生不利影响。
此外,IR方法的主要优势在于模拟数据与测得的原始数据之间的实际相关性,从而有效减少图像噪声和伪影,并实现相对较快的重建速度。同时,与FBP相比,IR保持了CT的衰减值,并保持了高图像质量和诊断置信度。此外,IR使得在肥胖患者或体型较大的患者中获得高质量的CT图像,并且使得在尿路结石患者中进行超低剂量(ULD)CT成为可能。
此外,在高对比度分辨率情景(例如肺实质评估)中,与FBP相比,IR算法可以实现高达70%的剂量减少而保持相当的图像质量。另一方面,高强度的IR在低对比度任务(例如小的低密度肝转移)中表现不佳,导致诊断准确性较低。即使在这种情况下,仍然可以达到10%至27%的剂量减少。然而,高强度IR数据集通常不被放射科医生所青睐,因为其重建时间相对较慢,而且对图像纹理有影响,导致过度平滑的 “塑料状 “图像可能会妨碍临床任务。
总之,通过增强基于软件的迭代图像重建的计算能力的进步,实现了显著的图像噪声减少、对比度细节轻微增加和图像伪影大幅减少,这些特性都是低剂量CT采集的固有特征。因此,技术人员、放射科医师和整个医疗团队有必要共同努力,将所有IR的优势应用于临床实践中。
02 供应商特定的IR方法
每个供应商都有不同的IR算法,从计算要求不高、在图像数据域中进行重建的算法,到在原始数据域中操作的算法;每种IR技术的工作方式不同,确切的算法都是专有的(表1)。
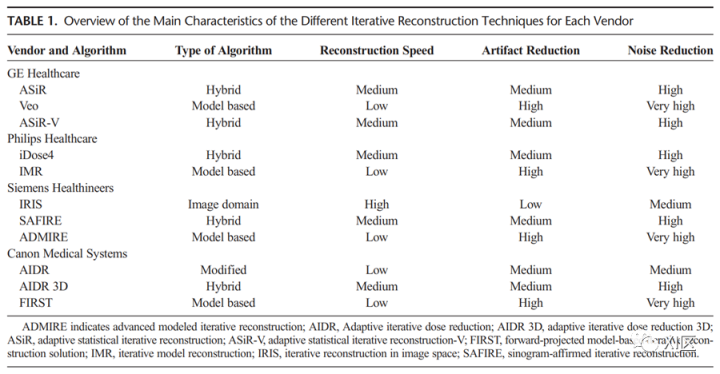
表1 每个供应商不同迭代重建技术的主要特征概述
2009年,Siemens Healthineers提出了第一个IR算法,IRIS,其仅在图像空间中使用迭代算法过滤器,达到降噪的目的。在IRIS之后,更先进的HIR算法被引入,如SAFIRE(sinogram-affirmed IR;Siemens Healthineers)、ASiR(adaptive statistical IR)和iDose4(Philips Healthcare)。另一方面,开发了MBIR算法,通过多次前向和后向重建进行操作:Veo (GE Healthcare), MBIR (GE Healthcare), ADMIRE (advanced modeled IR; Siemens Healthineers), FIRST (forwardprojected MBIR solution; Canon Medical Systems), 和IMR (iterative model reconstruction; Philips Healthcare)。
最近,基于神经网络的深度学习的图像重建(DLIR)算法正在出现:GE Healthcare的TrueFidelity(TF)和Canon Medical Systems的Advanced Intelligent Clear-IQ Engine(AiCE)。图2、3和4显示了用FBP、ASIR-V、TF和iDose4在不同水平上重建的CT扫描的例子。
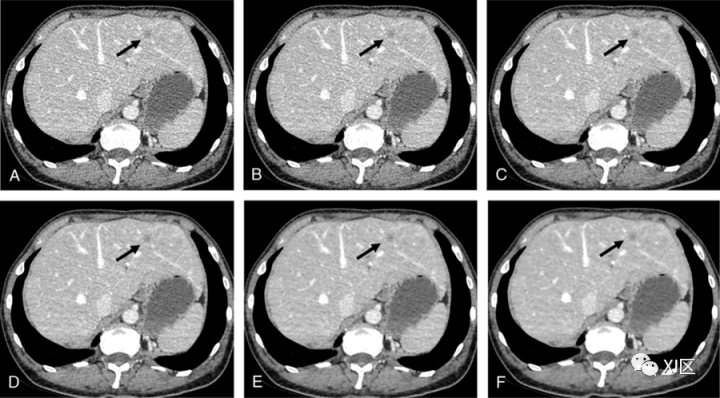
图2 用不同水平的ASiR-V算法重建的CT图像的比较。一位57岁女性,患有结直肠癌,伴有单肝转移,腹部静脉期轴位CT扫描(黑色箭头)。扫描是在100 kVp下通过管电流调制获得的(mAs范围,99–170);用(A)滤波反投影(FBP)和ASiR-V在20%(B)、40%(C)、60%(D)、80%(E)和100%(F)强度重建原始数据。随着ASiR-V强度水平的增加,图像噪声逐渐减少,而低衰减转移仍然可见。此外,IR在对比度可检测性和噪声降低方面的改进导致了腹部动脉和静脉分支的更好描绘,甚至是远端小血管的更好描绘。

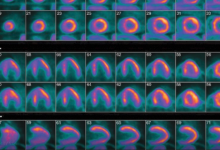
图3 用不同水平的ASiR-V和DLIR算法重建的CT图像的比较。一名82岁女性的轴位冠状动脉CT血管造影术扫描在100 kVp和200 mAs的固定管电流下进行。用ASiR-V 30%(A)、50%(B)和80%(C)的不同强度以及低(D)、中(E)和高(F)水平的DLIR重建扫描。中等强度水平(通常为50%至80%)的迭代重建显示图像噪声和图像质量之间的平衡得到了改善:特别是,IR显示血管细节的可视化更好,斑块轮廓的模糊程度更低。
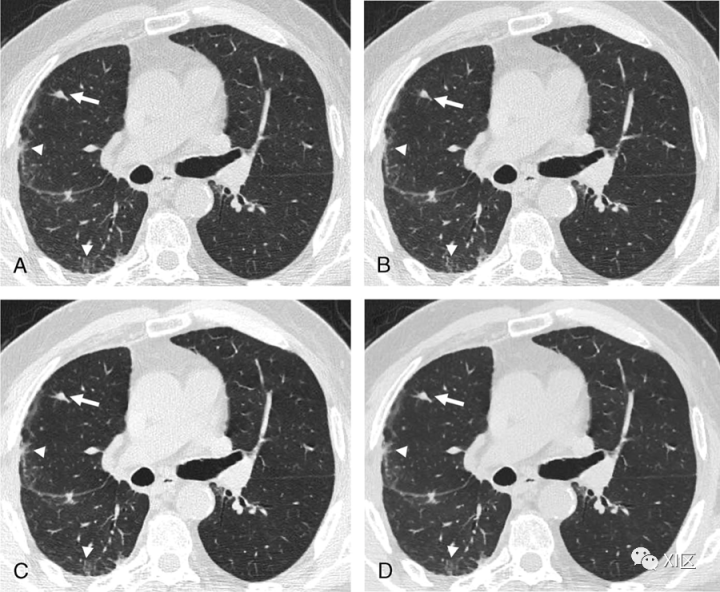
图4 用不同级别的iDose4算法重建的CT图像的比较。一名患有间皮瘤的63岁男子的轴向薄层非增强胸部CT扫描,显示右肺中有一个非钙化的实质结节(白色箭头)和胸膜下结构扭曲(白色箭头)。胸部CT是在100 kVp下采集的,具有管电流调制(mAs范围,109–220)。使用iDose4算法在不同水平重建图像:(A)iDose1、(B)iDoe3、(C)iDos5和(D)iDose7。高强度IR保持高对比度和空间分辨率,为减少辐射剂量铺平了道路。
GE医疗
ASiR(Adaptive Statistical Iterative Reconstruction)
ASiR于2008年推出,展示了在抑制图像噪声和伪影的同时降低剂量CT投影数据方面的良好效果。该算法利用从FBP算法获得的信息作为每个单独图像重建的构成要素。ASiR模型通过矩阵代数将每个像素的原始测量值转换为新的估计像素值,然后将其与通过噪声建模预测的理想值进行比较。该过程在连续的迭代步骤中重复进行,直到最终估计的像素值满足理想值。自适应统计IR可生成混合图像,其IR百分比从0%(FBP)到100%,间隔为10%,增加百分比与ASiR的贡献程度成正比。然而,较高强度的ASiR重建与IR特定伪影相关,表现为图像中的“塑料”纹理(不规则边缘、斑点、像素化)。
Veo
Veo是GE医疗公司推出的第二代IR算法,可以在1 mSv以下的CT扫描中实现出色的图像质量。该算法将数据采集过程的广泛三维模型与统计噪声和物理模型相结合,并反映由X射线和物质相互作用产生的数据的统计分布。在一个完整的迭代周期内更新图像体素,从而在单个图像中实现降噪和增加分辨率。然而,也发现了与复杂建模过程相关的几个缺点,例如需要非常高的计算能力和非常长的重建时间。
ASiR-V(Adaptive Statistical Iterative Reconstruction-V)
ASiR-V是由GE医疗公司推出的第三代IR算法,它是一种混合重建技术。与ASiR相比,ASiR-V改善了降噪和对象建模。它还应用了Veo中使用的部分物理模型,但在建模过程中排除了复杂的系统光学因素。因此,与Veo相比,ASiR-V的图像降噪潜力较低;然而,优势在于大幅减少图像重建时间。首先,ASiR-V对成像对象进行初始估计,然后根据实际测量的投影、先前的信息或特征对这个初始估计进行更新。对系统噪声统计、对象和物理的准确建模主要有助于降低与低剂量CT扫描固有的噪声和伪影相关的问题。
飞利浦医疗
iDose4
iDose4是由飞利浦医疗于2010年推出,它在图像质量方面提供了显著的改进,避免了早期IR技术所特有的“塑料”图像外观,这要归功于一种惩罚噪声数据并保留线性边缘的迭代过程。重建算法首先通过识别和校正最嘈杂的CT测量数据来处理投影数据;然后,可以根据所需的降噪水平去除剩余的噪声。iDose4的重建级别(从0到7)可以在扫描之前或在获取原始数据后选择。重建级别可以独立于扫描时的辐射剂量进行定义;然而,应根据所选择的剂量降低百分比来选择相应的iDose4水平。
IMR(Iterative Model Reconstruction)
IMR是飞利浦医疗在2012年推出,可以优化数据统计、图像统计和系统模型。它在控制图像噪声方面表现良好,在明显低于FBP重建的辐射剂量下最大限度地提高空间分辨率;此外,IMR在大多数CT方案中允许快速重建。事实上,与FBP和iDose4相比,IMR实现了图像质量的显著提高、图像噪声的减少和读者主观信心的改善,而剂量设置明显低于2 mSv。
西门子医疗
IRIS (IR in Image Space)
IRIS是西门子医疗在2008年推出的第一代IR算法。它只应用一次原始数据重建,然后生成一个包含原始数据信息总量的所谓 “主体积”,以加速重建的收敛,并避免漫长的重建时间。接下来的迭代校正会 “清理 “图像,在不降低图像清晰度的情况下去除噪声。因此,可以避免耗时的重复投影和相应的反投影。最终的结果是减少了伪影和噪声,提高了图像的清晰度,并且大大节省了辐射剂量。
SAFIRE(Sinogram-Affirmed IR)
SAFIRE是西门子医疗在2010年发布的第二代IR算法,它使用加权FBP进行初始重建,然后是两个不同的校正循环方法。第一个循环用于校正原始重建中的缺陷,并去除任何数据伪影;这个过程重复了一定的次数,期间应用了基于原始数据的动态噪声建模,从而促进了图像噪声的降低,而不会显著降低图像清晰度。第二个校正环路在图像空间上运行,通过多次重复的统计优化过程去除噪声。SAFIRE有5个强度级别,可以预览,其中降噪水平和图像纹理根据选定的强度级别而变化。
ADMIRE(Advanced Modeled IR)
ADMIRE是西门子医疗发布的第三代IR算法,是一种类似于SAFIRE的MBIR方法,但具有更好的边缘描绘和噪声纹理。该算法的特点是基于循环中使用加权FBP的多步骤过程,目的是消除几何缺陷,如锥束伪影;统计建模进行局部信噪比(SNR)分析,将数据分解为信号和噪声。前向投影步骤产生人工数据,与测量的原始数据反复比较。这主要有助于消除螺旋形伪影,并在较小程度上降低噪声。噪声主要通过包含于图像空间的正则化函数的第二步骤来减少。ADMIRE只需要少量迭代,因此重建速度很快。可以根据放射科医生的喜好选择五个可调节的强度级别,而不影响重建速度。
佳能医疗
AIDR(Adaptive Iterative Dose Reduction)
AIDR是佳能医疗开发的第一个IR算法,图像降噪发生在重建图像领域。这种IR技术要求原始的高噪声图像经过几次循环迭代来降低图像噪声,直到达到理想的噪声水平。
AIDR3D(Adaptive Iterative Dose Reduction 3D)
该系统采用三维处理的重建算法,结合了原始数据和图像空间的噪声优化。AIDR3D能够根据特征体素梯度降低噪声,保持主要的精细图像细节,如线条和边缘。在每次迭代中,AIDR3D能够平衡降低噪声幅度和保留空间分辨率之间的关系;原始FBP图像被用作每次迭代的输入,并与处理后的数据混合,形成最终的图像,确保噪声纹理得到很好的保持。AIDR3D能够根据身体区域和检查类型自动调整算法,确保参数和图像质量优化。也可以让操作者对算法和可调强度进行一些控制。
FIRST(Forward-Projected MBIR Solution)
前向投影MBIR解决方案是建立在FBP基础上的一种混合算法。然后,佳能医疗推出了真正的前向投影MBIR。前向投影MBIR解决方案在每次迭代中都要进行前向投影,根据扫描过程中获得的测量的原始投影数据,制定一个图像(”种子图像”)的初始 “猜测”,在创建一组新的合成投影数据之前对其进行处理,并送入IR循环。然后,种子图像通过一个数学比较引擎进行渗透,以评估合成的前向投影和原始投影数据之间的差异。因此,更新的合成投影应该用反投影进行阐述,以产生新的图像。这个过程必须重复进行,直到达到理想的图像,在前向投影过程中使用复杂的模型,确保前向投影的MBIR减少图像噪声,同时提高对比度空间分辨率。
DLIR技术
GE医疗-TrueFidelity
为了克服IR本身的建模限制,GE Healthcare开发了一种名为TrueFidelity的DLIR算法。DLIR的力量在于其处理复杂模型和大量参数的能力,远远超过人类的能力。计算机同时训练数以百万计的参数,通过训练过程直接生成真实的系统模型。TF图像的结果在降噪、空间分辨率和可检测性方面有所改善,而图像纹理的变化较小。有希望的结果鼓励在临床实践中进一步应用剂量优化的CT采集,这一点尚未被HIR有效解决。
佳能医疗-AiCE
佳能医疗开发的新算法Advanced Intelligent Clear-IQ Engine使用深度卷积神经网络,通过将结果与通过MBIR重建的参考标准高质量数据进行比较,学习从低质量数据中创建高质量结果。
2018年商业化的第一个版本(AiCE V8)有一些局限性,因为只考虑了0.5毫米的切片厚度和只有3个卷积核(体部、肺和心脏)。最新的版本(AiCE V10)允许在不同的切片厚度(0.5、1.0和2.0毫米)和5个额外的重建核进行图像重建。
其结果是一个完全集成的DLIR,可以区分和减少信号中的噪声,从而在日常工作流程中提供诊断图像质量,同时保持尽可能低的辐射剂量。
03临床应用
肿瘤
增强CT(CECT)成像被认为是肿瘤患者管理的标准检查,用于诊断、分期和监测治疗反应;在这场竞赛中,IR算法在低辐射剂量下保持图像质量和诊断信心方面发挥了关键作用,以遵守 “ALARA “原则。
Morimoto等人进行了一项前瞻性研究,比较了ASiR重建的低剂量CT图像与FBP重建的标准剂量(SD)CT图像在进行胸腹部CT随访的肿瘤患者中的图像质量和病变显著性。低剂量CT显示出更高的整体图像质量、更低的图像噪声和更好的病变清晰性,实现了中位辐射剂量减少46%。
Nagayama等人进行了一项回顾性研究,对两组不同CT协议进行了比较:第1组接受LD低对比剂(CM)CT(360 mgl kg-1, 80 kVp, SAFIRE),第2组接受SD、常规CM CT(600 mgl kg-1, 120 kVp, FBP),第一组方案使剂量减少32%,碘负荷降低40%,客观图像质量更高,主观图像质量相当;此外,没有记录到与CM注射有关的明显的肾脏损伤。
Ippolito及其同事比较了分别用MBIR和HIR算法重建的LD(100 kVp)和SD(120 kVp)增强CT图像的图像质量和辐射剂量。与HIR相比,用MBIR算法重建的CT图像的整体图像质量、SNR和对比度-噪声比(CNR)值明显较高,而辐射剂量则明显较低。
肝脏病变,特别是低密度的转移,值得单独提及,因为它们在用高强度IR重建的LD CT中经常会被误诊。许多作者已经证明,主观的图像质量并不一定与诊断准确性的提高相关;事实上,IR并不能保持低对比度的可检测性,不同剂量水平的IR方法在低对比度检测方面存在很大差异。Dimmitt等人评估了使用ASiR-V与FBP对比检测肝脏病变的诊断准确性,证明ASiR-V客观上优于FBP,尽管读者使用FBP可以更好地识别肝脏病变。因此,读者应该进行充分的培训以避免任何肝脏病变的误诊。此外,Mohammadinejad和他的同事表明,IR应用于肝脏多相CECT可以稍微改变图像质量。然而,一项比较研究表明,使用FBP和SAFIRE在不同强度下重建CECT腹部扫描,图像噪声随着IR水平的提高而降低,可以更好地观察到小的低衰减的肝脏病变。
筛查
超低剂量(ULD)检查是筛查方案中不可避免的要求,它代表了IR技术的主要应用领域之一,特别是肺癌筛查。
Zhang及其同事使用ULD协议(120 kVp/17 mAs)和常规LD(120 kVp/30 mAs)比较了胸部CT图像质量和结节可检测性,两者均采用FBP、iDose4和IMR算法进行重建。与LD方案相比,ULD可以有效减少剂量(44%;0.67 vs 1.20 mSv);此外,在这两组中,IMR显示出比HIR和FBP更好的图像质量、结节可检测性和图像噪声降低。
de Margerie-Mellon等人比较了接受HIR重建的SD CT(140 kVp)和使用FBP、iDose4和IMR重建的低剂量CT(100 kVp)的患者中IR和FBP的性能。有趣的是,与FBP相比,iDose4和MIR显示出更好的诊断可信度、病变明显性和肺气肿检测,且剂量明显较低(中值分别为0.22和1.8 mSv)。
CT结肠造影(CTC)的临床适用性在过去十年中逐步发展,以至于被认为是结直肠疾病的有效检查。Cianci等人评估了用SAFIRE重建的ULD-CTC的辐射剂量和图像质量,与用FBP重建的LD-CTC相比。结果显示,与LD-CTC相比,ULD-CTC方案有意义地减少了剂量(高达63%;分别为0.98 vs 2.69 mSv),但既没有明显的图像质量下降,也没有影响病变检测。
Liu及其同事评估了3组CTC筛查的图像质量、辐射剂量和诊断性能:SD(120kVp-STD,FBP)、锡滤过LD(Sn150kVp-LD,ADMIRE)和锡滤过ULD(Sn100kVp-ULD,ADMIRE)。与120kVp-STD方案相比,Sn150kVp-LD和Sn100kVp-ULD组的图像质量更好,辐射剂量分别降低了22.5%和87.5%。
心血管
心血管放射学是最受益于IR的放射学领域之一,特别是在门急诊病人中。
Si-Mohamed及其同事比较了使用SAFIRE的100kVp和使用FBP的120kVp的 “胸痛三联 “CT血管成像(TRO-CTA)的诊断性能。与SD TRO-CTA方案相比,低剂量TRO-CTA可以在减少34%辐射剂量的情况下达到高置信度的诊断水平。
Ippolito等人评估了使用MBIR重建的LD冠状动脉CT A(CCTA)检查的图像质量和辐射剂量,并与标准iDose4 CCTA重建进行了比较。结果表明,与标准CCTA方案相比,LD MBIR CCTA可以获得高质量的图像,并显著减少剂量暴露(38%)。
Talei Franzesi及其同事评估并比较了2种不同的研究方案:LD和低CM量的CT A方案(100 kVp;50 mL的CM;IR算法)和标准CT A方案(120 kVp;100 mL的CM;FBP重建)。在相当的图像质量下,与标准CTA方案相比,LD-CTA可以显著减少辐射剂量(20%)和CM体积。
Caruso及其同事分析了由FBP重建的SD(120 kVp,170 mAs)和由ASiR重建的半剂量(120 kVp,85 mAs)在不同强度水平下的冠状动脉钙化评分方案。结果表明,与FBP相比,ASiR-70%显示出更高的信噪比和CNR,半剂量方案提供的辐射剂量减少了52%,但对主观分析没有明显影响。
儿科
儿童对电离辐射的随机效应更加敏感,不幸的是,由于非儿科医院普遍使用 “成人 “CT方案,儿童可能会接受更高的有效剂量;LD-CT与IR技术相结合,在儿科应用中可以大幅减少辐射剂量,同时提高图像质量。
Singh等人调查了用ASiR重建的胸部和腹部CT数据的图像质量和辐射剂量的减少,与传统的FBP相比,证明胸部CT的剂量减少了46%,腹部CT减少了38%,客观噪声更少。
Zhu等人分析了急性头部创伤儿童的CT剂量指数和图像质量,分为1组(低剂量CT:100 kVp/240 mA,ASiR-V 70%)和2组(SD CT:120 kVp/180 mA,FBP)。与第二组相比,第一组实现了37%的辐射剂量减少。
Yamasaki及其同事比较了接受CTA的婴儿的FBP、HIR和MBIR,发现与HIR相比,MBIR的辐射剂量明显降低(36%),与FBP重建相比,MBIR的平均CNR更高(高达41%)。
Sun及其同事评估了MBIR和ASiR的性能,与FBP重建相比,在LD和低CM体积的腹部CECT中,证明如果结合ASiR 100%(降噪,63%;CNR,高达151%)和MBIR,LD-CT的图像质量会更好,后者的性能最好(降噪,67%;CNR,高达171%)。
头颈
Bodelle等人证明,与在类似管电流下获得的FBP方案相比,用SAFIRE重建的LD-CT改善了颅内出血的检测,剂量减少了29%(1.71 vs 2.4 mSv)。
Paprottka及其同事分析了分别使用iDose4和IMR算法重建的SD和LD大脑CT平扫。与SD相比,LD-CT显示出明显的剂量减少(33%,31.2 vs 46.6mGy),并且图像质量更好。
Troeltzsch等人评估了CT金属伪影减少技术的好处,发现IR和金属伪影减少技术提高了头颈部CT对原发肿瘤(敏感性,0.83;特异性,0.93)和复发肿瘤(敏感性,0.94;特异性,0.93)的诊断质量。
Schmid及其同事检查并比较了用单源CT(固定管电压,120 kVp;FBP和SAFIRE)和双源CT(自动管电压调制,FBP和ADMIRE)获得的图像。与FBP相比,两种IR技术都显示出较低的图像噪声、较高的信噪比和CNR,以及更好的主观图像分析;此外,ADMIRE显示出比SAFIRE低14.4%的图像噪声和7.5%的辐射剂量。
04 未来展望
人类社会对辐射引发肿瘤的担忧,导致CT诊断成像数量有所下降。尽管成为标准的重建技术,但IR存在一些缺点,如过度平滑的图像纹理和适度的剂量减少与对比度依赖的空间分辨率有关;因此,成像重建技术有很大的改进空间。
在过去的几年里,人工智能在图像纹理、剂量优化、计算机辅助诊断以及通过减少伪影和图像噪声来提高整体图像质量方面显示出一种很有前途的工具。
最近,一些研究正在调查DLIR算法在进一步减少辐射剂量,同时保持诊断图像质量方面的作用,与IR技术相比,取得了积极的结果。Bernard及其同事在CCTA急性卒中方案中,使用DLIR算法与HIR算法相比,剂量明显减少(约40%),SNR(51%)和CNR(49%)更高。对LD CCTA扫描也有类似的结果:与ASiR-V-100%相比,DLIR-H可以减少43%的辐射剂量,但对图像噪声、狭窄严重程度、斑块组成和斑块体积定量评估没有明显影响。Kim等人的一项回顾性研究显示,与ASiR-V技术相比,用DLIR重建的LD胸部CT用于肺癌筛查,可以明显降低噪声,提高SNR和CNR,提高图像对比度,降低图像噪声,更好地识别结构。Jensen等人在对40名接受腹部CECT检查的肿瘤患者进行的回顾性研究中表明,与ASiR-V相比,DLIR具有更好的CNR,噪声降低了47%,并提高了整体图像质量和病变诊断的可信度。
在不久的将来,人工智能技术可能提高放射学检查的性能和速度,实现ULD CT扫描。然而,要充分发挥人工智能的潜力,这些技术需要大规模的验证和进一步的分析。
05 结论
限制剂量暴露是管理各类患者的一项具有挑战性的任务,特别是对于需要持续进行多次CT检查的肿瘤患者。在过去的几十年里,由于数学和信息学领域的进步,医学成像发生了深刻的变化;IR代表了硬件和软件发展的主要成果之一:能够在大幅降低剂量的同时提高CT诊断能力,目前已广泛取代FBP成为CT图像的标准重建模式。放射科医生必须了解IR技术,以便在日常临床实践中最大限度地发挥其潜力。此外,关于人工智能重建算法的初步有数据正在出现;在可预见的未来,成像重建领域有望取得进一步的进展。