前面第一部分叙述了PET早期发展阶段进行的符合测量,从正电子扫描机、正电子照相机发展到正电子发射计算机断层仪的艰难历程。接下来我们对PET仪的完善和进一步的发展进行回顾。
1、早期的研究
1970s初英国EMI公司工程师Hounsfield(豪斯菲尔德)发明x射线计算机断层摄影,因为此项贡献而与科马克分享1979年诺贝尔生理学和医学奖。几乎在同一时期, Kuhl等对单光子发射计算机断层扫描(SPECT)进行研究。并由布丁格和古尔伯格扩展应用到正电子发射断层。 切斯勒将MGH正电子照相机进行旋转并记录多个视图,然后将这些视图滤波反投影,获得跨轴断层图像。Chesler用外部Ga源 记录透射图像,为每个投影提供符合检测器之间每条响应线的精确衰减校正,并在1971年加州洛杉矶第18届美国医学年会上首次报道,1972年核医学会议上详细陈述。这一方法提供了避免重建图像失真,以及定量组织放射性浓度的方法。1973年,Chesler展示了心肌灌注的断层图像。
1974年密苏里州圣路易斯,特-波高斯、菲尔普斯、霍夫曼和穆拉尼重新研究了正电子断层扫描仪的物理特性,以确保能够量化组织局部示踪剂的浓度。他们专注于优化扫描仪的物理设计,以最大限度地减少由于随机和散射事件以及死时间而导致的失真,设计了六边形碘化钠闪烁探测器阵列。与MGH正电子照相机一样,在每个探测器的前面放置了铅制的栅,以提高空间分辨率。为了确保采集足够的信息,他们以间断移动检测器,并围绕跨轴平面递增旋转,该系统被称为正电子发射跨轴断层成像(PETT)。这个工作的主要贡献是能够定量测定局部组织的正电子放射性核素浓度,这些定量测量被认为是正电子断层成像的重要特性,图像上的组织摄取可以用放射性的绝对单位进行校准。这通过交叉校准充满放射性液体的体模来实现,该体模在扫描仪中成像,并使用从体模中取出的等分试样样本在井计数器或剂量校准器中测量。然后,组织的示踪剂浓度可以用与给药剂量相同的单位来测量。示踪剂的血液浓度可以从图像内的血池区域获得,或者取自计数器测量的患者血液样本。通过校准的注射剂量、血液和组织浓度的测量值,示踪剂的生物分布可以相对于给药剂量和血液浓度进行量化。通过摄取示踪剂期间获得一组连续的时间帧,可以模拟血液和组织之间示踪剂交换的动力学,以导出交换速率常数。这些常数与被追踪的生物途径的代谢率和组织内分子交换位点的活性密度直接相关。PET在体内无创地进行绝对测量的能力是独一无二的,也是临床研究和医疗保健的主要优势。霍夫曼等发表了一系列关于用正电子发射仪获取定量资料的论文。
2、PET的第一次突破:从局部显像到全身成像
上世纪80年代前, PET研究集中在中枢神经系统(脑)和心脏,PET轴向视野的范围也限于这些器官,数据采集只一般需要一个床位。
从圣路易斯搬到费城的库尔后,菲尔普斯和霍夫曼与道格拉斯和威廉姆斯与位于田纳西州橡树岭的EG & G ORTEC公司合作。这一合作的主要成果是产生了一种商业的单轴平面正电子断层扫描仪,被称为发射计算机化轴向断层扫描仪,即ECAT I,它也由六边形探测器阵列组成。这种商业设计的第一个版本安装在洛杉矶加州大学洛杉矶分校,展示了用F-FDG记录的令人信服的大脑图像。该设备后来升级为ECAT II,如图10(a)所示,由欧洲、美国和日本的一些已经装备了回旋加速器的中心购买。该设计使用标准化的、商业支持的PET扫描仪启动了许多基于PET的临床研究项目。
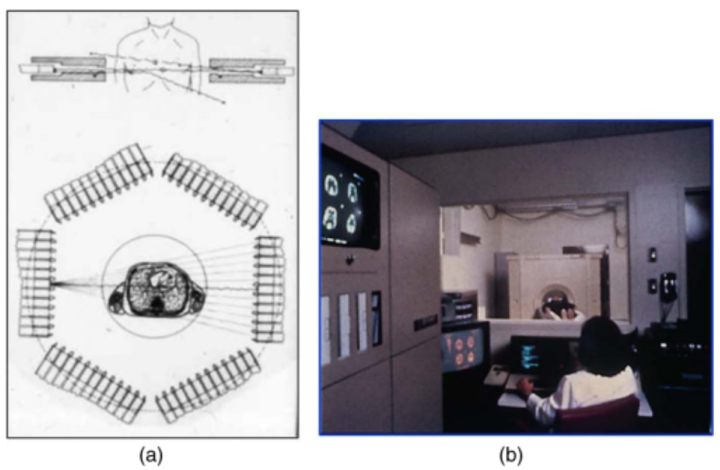
图10 田纳西州橡树岭EG & G ORTEC公司开发的ECAT II扫描仪示意图
显示早期PET扫描仪的有限立体角覆盖;这一设计基于特-波高斯和他的同事在圣路易斯开发的PET III,以及(b)在加州大学洛杉矶分校展示的第一台商用PET扫描仪ECATI
下一个引入的设计是基于环形的几何结构,由于探测器元件的尺寸和间距,需要创新以获得足够的空间采样。通过晶体旋转和整个探测器环的摆动来实现。摆动模式要求断层扫描仪中心移动到圆周1英寸的四个特定位置。在每个位置采集完整的发射数据集,从而在整个视场中采样不同的响应线。然后,这四个集合可以被分类成平行投影,其中投影采样高于任何一个单独的采集。这些早期的设计结合了闪烁晶体和光电探测器(通常是光电倍增管)之间的一对一耦合。这种光电探测器使多个跨轴平面的组装变得复杂,而这些平面将成像扩展的轴向覆盖范围。成功完成的神经造影仪由三个八边形锗酸铋(BGO)探测器阵列组成,产生了同时成像的五个跨轴平面。随后产生的是ECAT III,它包含了三个主要为心脏成像设计的探测器环。ECAT III中包含的较小晶体尺寸产生了足够讯号采集,从而消除了旋转或摆动环的需要。由卡罗林斯卡学院的埃里克森与乌普萨拉的斯坎蒂罗尼克斯公司共同开创的另一项创新是旨在产生更高分辨率的设计。它包括将两个闪烁晶体,一个BGO和一个正硅酸钆(GSO)耦合到一个光电倍增管。
由于正电子断层扫描仪的典型轴向覆盖范围是16到25厘米,为了进行F-FDG全身成像,患者必须轴向移动通过扫描仪的视野。这种多步骤成像方案的可行性最初是由达尔博姆等人在加州大学洛杉矶分校证明的(图11 )。

图11 通过以不连续的重叠步进移动床来获得患者的全身图像;按照患者身长,以5至7个床位置覆盖从脑底部到大腿的范围。
检查床连续移动、扫描时床位之间部分互相重叠等的引入实现了PET全身显像。这时专家就已经预测:PET全身扫描的比重还会增加,它在检测一些基因分子、DNA/RNA或者免疫作用的治疗,以及感染性疾病、不稳定斑块及炎症疾病中会起到关键作用。
3、PET的第二次突破:从二维到三维
在进行全身显像的初期,PET以二维方式采集数据,使用BGO晶体(鍺酸铋,Bismuth Germanate,BGO)。BGO晶体阻截511kev光子的能力强,但是散射分数较高,时间分辨率差(300ns)。需要在相邻的晶体环之间按装可以自动伸缩的铅栅,用来减少来自于周围晶体环的散射线。进行二维方式数据采集时,铅栅伸出,使同一个或相近的湮没辐射(Annihilation)被接受并形成有效符合,灵敏度、散射分数、随机符合低。早期进行全身显像需要近一小时左右,患者不适,图像不够满意。临床实践认为二维数据采集方式适合于局部显像,如心脏和脑。核医学临床需要扫描速度更快、散射和随机符合较低、图像质量更好的PET系统。三维数据采集PET系统和新晶体的研发应运而生。由于受试者全身接受辐射剂量,不管身体部位是否在成像视野内,扩大轴向覆盖范围将更好地利用光子通量,并提高整体系统灵敏度。Anger伽马照相机中首创的光电倍增器之间光共享方法克服了环形系统中一对一耦合的限制,在MGH正电子照相机的构造中采用了该方法。使用这种光共享技术,Casey和Nutt开发了块检测器,该检测器由耦合到晶体元件的8×4 (32)阵列的四个光电倍增器组成,每个晶体元件5.6X12.9X30毫米。使用的闪烁晶体是BGO,它不仅比以前使用的碘化钠密度大,而且不吸水,因此更容易组装。图12显示了耦合到四个光电倍增器的8×8 (64)阵列的块检测器原理。
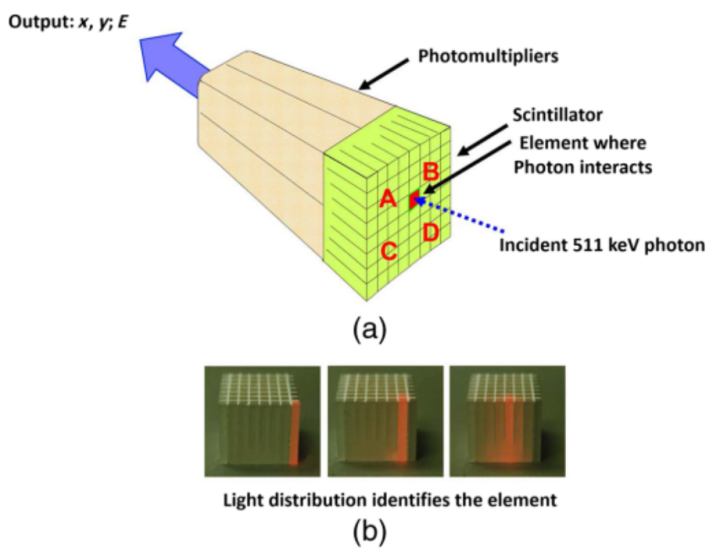
图12 凯西和纳特1985年提出块探测器
入射湮灭光子在闪烁体中被转换,四个光电倍增管之间的光共享(b)识别闪烁体元件并定位入射光子。块探测器的输出坐标(x,y)和光子的能量(E),光子能量通过对闪烁体中产生光的求和而获得
伦敦哈默史密斯集团收购了第一台商用块探测器PET仪,最初设计在探测器的多个环之间加入薄的钨片,称为隔栅。隔栅将光子的探测限制在给定的探测器平面内和任一侧的一个相邻平面内,这样,三维活动体积基本上被成像为一组二维平行的跨轴平面。虽然隔栅减少了系统死区时间,并限制了对来自其他区域的随机和散射,但真实符合的接受角小,导致整体灵敏度非常低。哈默史密斯公司临时移除了扫描仪中的隔栅,提高了灵敏度,证明了三维(3-D)重建的能力,从而导致了新一代的PET扫描仪的设计。如图13所示。
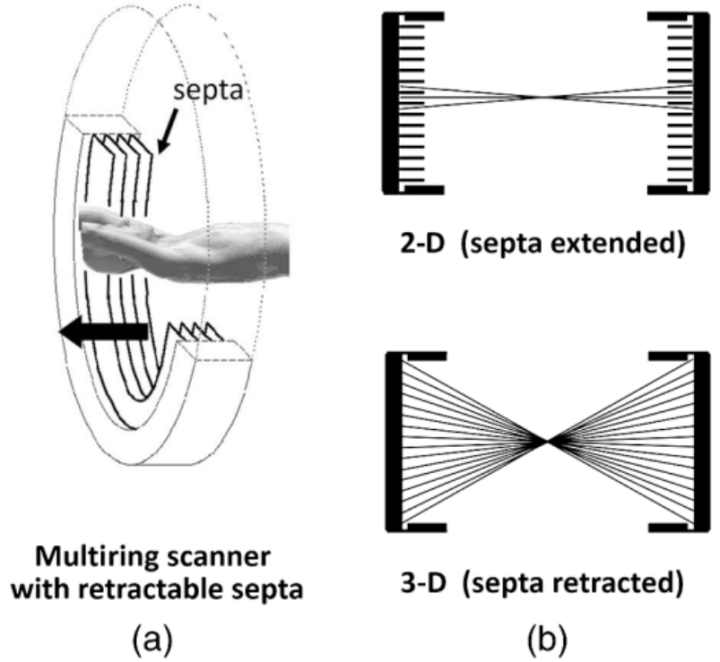
图13 二维和三维正电子发射断层扫描采集几何图形示意
最初的多环正电子断层扫描仪配置(a)在探测器环之间结合了铅或钨屏蔽,从而将采集限制在每个环内的正电子;隔栅消除了视野外光子。移除隔栅后,(b)可以进行全三维采集,包括视野内和视野外光子。
1991年,在哈默史密斯回旋加速器装置上安装了第一台这种带有可伸缩隔栅的扫描仪作脑显像。在此基础上设计的扫描仪,使用两组相对的BGO块检测器,不用隔栅,围绕患者旋转以获取完整的三维数据集。 20世纪80年代和90年代的大部分时间里,BGO是CTI公司(与西门子医疗保健公司合资)和通用电气公司的PET仪中使用的主要闪烁体。凯西和纳特首创的积木设计被提炼成不同的晶体矩阵,与四个光电管相连。特别是,ECAT HR 47由8×7个大小为5.9毫米×2.9毫米的晶体组成,并成为临床正电子发射断层显像的主力,ECAT HR+由8×8个4.4毫米×4.2毫米的晶体组成,用于高分辨率脑和全身成像。
上世纪九十年代后期的三维PET系统去除了早期二维PET中使用的铅栅,使得探测环之间也可以发生符合事件,这样就在没有增加晶体容量的前提下,使得灵敏度提高了5~7倍。如今,基本上所有商用的PET扫描仪都是以高灵敏度的三维模式收集数据,在任何情况下都不配备隔垫。由于散射分数可以达到35%或更高,已经开发了复杂的散射校正模型来解决这个问题。博格斯特伦等人基于投影数据的积分变换开发了早期的二维散射校正技术。三维正电子发射显示器的出现需要不同的方法,第一种方法是贝利和米克尔的卷积相减法。这种方法后来被最初由奥林格开发并由沃森等人独立开发的单一散射模型所取代。该模型使用(未校正的)发射活动分布和衰减介质图来估计散射分布。
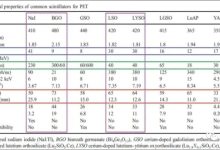
4、晶体的变革
三维采集的广泛采用挑战了BGO的极限,尤其是对病人的全身成像。需要寻找一种具有更好的光输出、更快的上升和衰减时间、更高的能量分辨率和更短停滞时间的闪烁体。为了实现空间分辨率的提高,检测器块需要被细分成更精细的元件阵列,因此,需要增加光输出,以便正确地识别检测器元件而没有明显的误定位。更高的光输出也将提高能量分辨率,从而更有效地抑制散射事件。 这项研究引出了一种新的闪烁体——硅酸镥(LSO),发现它在正电子发射成像方面具有比BGO优越得多的光发射特性。1999年左右出现的ECAT ACCEL48是第一台使用LSO的商用正电子发射仪。LSO也是用于脑部成像的高分辨率研究断层扫描仪(HRRT)中的闪烁体。有一些供应商使用了掺有少量钇(LYSO)的LSO的衍生物。而飞利浦医疗保健公司推出了使用GSO作为闪烁体的正电子断层扫描仪(Allegro)。这些新闪烁体的技术优势使得能量分辨率更高,从而导致探测器块中更精细的细分(13×13)和更低的散射分数,以及更高的时间分辨率,从而导致更低的随机符合率。
新一代的PET系统,脉冲可以叠加在更短的时间内,三维 PET高灵敏度带来的优势得到更好的体现。市场上以往的BGO晶体系统,较高的散射分数的和较宽随机符合时间窗对图像质量的提升造成很大障碍。BGO晶体必然退出历史舞台。
5、第三次突破: 从三维PET到四维“飞行时间”PET
成对的两个511KeV湮没辐射光子在预设的符合时间窗内被探测,被认为发生一个“有效事件”。正电子湮没辐射发生的原始位置,在射线命中的两块晶体所连成的响应线(LOR)上。但具体在响应线上哪个位置,要通过图像重建才能确定。由于没有任何其他信息提供,重建算法在进行起始重建时,被迫假定湮没位置在响应线所有位置的概率是同样的,这样就相当于把许多正确的信息放在错误位置上,由此导致了大量的噪声。 在TOF PET中,两个湮没辐射的光子到达晶体的实际时间差可以被测量并记录,距离响应线中心位置越远,两个光子到达晶体的时间差越大。利用该时间差,理论上可以确定湮没辐射的位置。但由于系统时间响应有一定的误差,因此所确定的湮没辐射的位置也不是一个精确的点,只能限定在以该点为中心的一定范围。但即便如此仍可对重建参数进行约束,将湮没辐射位置初步确定在数厘米范围内,进而对该事件的重建信息(位置、浓度)可以进行更合理的权重分配。
其实TOF PET是上世纪八十年代中期热烈讨论并且被遗弃的老概念,为什么二十多年后TOF PET又“热”起来了呢?关键在于目前的TOF PET使用了新的晶体和超高速电路。在上个世纪九十年代,业界当时能获得的具有较好时间分辨率的晶体是BaF2(氟化钡)和CsF(氟化铯),这两种晶体的PET系统时间分辨率为550–750 ps 。但这些晶体在时间分辨率方面得到的信噪比提升,远抵不上它们的低探测效率(与BGO晶体相比较,相同放射性药物量,其计数、信噪比低)导致的信噪比损失。同时这些早期系统的稳定性也不如人意。近来研究发现新一代晶体如LSO和LYSO 具有良好的时间分辨率,阻止光子的性能优异,探测效率一流,因此,TOF技术重新复活是技术发展的必然。
上世纪九十年代早期就强烈意识到PET成像受限于其二维采集方式的低灵敏度,但对PET晶体的选择困难。当时可供选择的晶体包括NaI(Tl)和 BGO(鍺酸铋,Bismuth Germanate,BGO),前者传统上用于伽马相机。两者的特性都不理想。BGO有较高的阻止性能,对511KeV光子提供好的探测效率,但衰减时间较慢和光输出量较低导致其时间分辨率和能量分辨较差。BGO晶体的PET系统在三维模式上图像质量明显受限于其过长的死时间、高随机符合和高散射。NaI(Tl) 晶体能量分辨率很好(因此可以使用高能窗减少三维数据中的散射成分),并且成功应用到了数个纯三维系统中,但其时间分辨率仍然相对较差,死时间长,阻止性能也相对比BGO要差。新的晶体材料,尤其是LSO【Cerium doped lutetium oxyorthosilicate(铈)硅酸镥】 及其相关的如LYSO【Cerium and yttrium doped lutetium oxyorthosilicate(钇、铈)硅酸镥】 ,就成为一大突破。这些晶体密度高,更透明,更快,拥有杰出的时间分辨率和良好的能量分辨率,并且这些晶体的阻止性能比BGO只差一点。这些良好的晶体特点结合快速电路,显著提高了三维 PET扫描仪系统的性能。由于这些晶体比BGO透明,因此允许每个光电倍增管(PMT)解码定位更多的晶体探测单元,这样就部分地控制了在PET系统使用更多的晶体导致的成本增加。
除了更高的光输出导致更好的空间和能量分辨率之外,LSO的一个主要优点是更快的定时,这导致更低的检测器死时间,并且最重要的是,能够测量检测器中两个湮灭光子到达之间的时间差。这种能力被称为飞行时间(TOF),它为湮灭点提供定位信息,没有飞行时间就无法获得这些信息。通过对湮灭点的定位、定时信息转化为统计增益,从而降低图像中的噪声。20世纪80年代,人们曾用快速但停止能力低的闪烁体探索过飞行时间;对于传统的飞行时间成像来说,BGO太慢了。然而,直到LSO出现后,飞行时间才随着飞利浦 “双子座飞行工具(True Flight)”的推出而复苏。西门子Biograph 6 Truepoint上进行的一项研究表明,通过降低图像噪声,可以提高病变的可检测性,特别是对于体重指数> 30的患者。如今,所有使用快速闪烁体的正电子发射断层扫描仪都将飞行时间集成到重建算法中,对于基于光电倍增管的探测器,其时间分辨率约为500 ps,对于采用新型固态光电探测器的探测器,其时间分辨率低于400 ps。显示图像数据的改进极大地促进了PET的广泛应用。
新晶体的出现重启了TOF技术,提高了PET图像的质量,不断缩小晶体、光电倍增管、电路及附属部分的时间损耗,提高整体的时间分辨能力,提升PET的信噪比和分辨率。
TOF PET系统最大的优势在于提高了系统的信噪比。TOF PET对信噪比的提升程度超过了引入三维 PET后的效果,使显像更快、注射剂量更低、信噪比或临床图像的分辨率更高。TOF PET对图像质量的改进对肥胖患者更显著。
6、第四次突破:全身PET/CT(全身PET/ MRI)
国家癌症研究所资助下,美国儿科学会创新中心(田纳西州诺克斯维尔)和匹兹堡大学合作1987年开发了一种原型PET/CT仪,并于1998年开始在匹兹堡大学医学中心进行临床评估。同年,医疗保险批准了一些PET项目的报销。尽管匹兹堡原型被设计成在单个设备中执行临床CT和临床PET成像,但另一个优点是CT可用于提供PET数据所需的衰减校正因子。临床对PET/CT原型的兴趣最初遭遇到一些热情的支持和相当保守的反对。然而,早期的PET/CT扫描结果足以激发通用电气公司和西门子公司在2001年的几个月内开发出商业设计。改进的PET成像能力和CT的使用在几秒钟内提供PET衰减校正因子,而不是以前所需要的数分钟。与以前的PET扫描仪相比,大大提高了患者的处理量。由于越来越多的肿瘤学适应证的正电子发射断层扫描得以报销;扫描时间的缩短,使患者处理量提高,提升了医院的经济效益。PET/CT融合图像通过将PET的代谢数据与CT解剖结构相结合,极大地提升了图像信息,提供了更精确的疾病分期和更好的诊断。2004年,飞利浦也加入了提供PET/CT扫描仪的公司行列。过去几十年中,随着多层螺旋CT的引入和采集、重建和显示软件的改进,主要供应商一直在继续开发PET/CT技术。最近,东芝美国医疗系统公司(现在的佳能公司)的Celesteion正电子发射断层扫描系统进入美国市场;上海的联影公司,推出了一种高分辨率正电子发射断层扫描系统(uMI 510),具有592个LYSO晶体。
早在上世纪60年代,科学家就对融合不同的成像方式以获得更完整的疾病图像感兴趣, 到了90年代这种需要更迫切。由于成像设备是各自分开的,通常属于不同的临床部门,需要通过日益复杂的软件来实现不同模式的影像融合。由于大脑固定于颅骨内,活动(移动)的自由度非常有限,因此在大脑图像融合中达到了高精度。而身体其他部分问题要复杂得多,因为与大脑相比,其他器官和结构的固定不动的难度要大得多。这个问题被多模态成像的先驱,来自UCSF的已故Bruce Hasegawa认识,他在1991年第一次采用两种SPECT和CT成像方式的“硬件”融合。也是在1991年,Townsend和Nutt提议将正电子发射断层成像与X射线断层成像结合,尽管他们不知道,大约7年前(1984年)日本群马大学的盖娜教授等人已经开发了正电子发射断层成像/断层成像设计。该设计包括一个并行的PET和一个CT扫描仪,其中一张床安装在一个平台上,该平台横向移动,与扫描仪机架平行。该平台将床从一个扫描仪传送到另一个扫描仪,并允许在患者不离开床的情况下采集共配准的正电子断层扫描和X计算机断层扫描图像。相比之下,汤森和纳特提出的设计将正电子断层扫描仪和x光计算机断层扫描仪结合成一个单一的设备(图14),既能对解剖结构成像,又能对功能成像。潜在的概念是提供一个精确的高分辨率的断层扫描解剖框架,用于低分辨率的功能成像。由于患者可以通过组合装置进行平移,因此即使依次采集了断层扫描和正电子断层扫描,也可以在一次检查中获得患者移动最少的完整全身正电子断层扫描/X断层扫描。
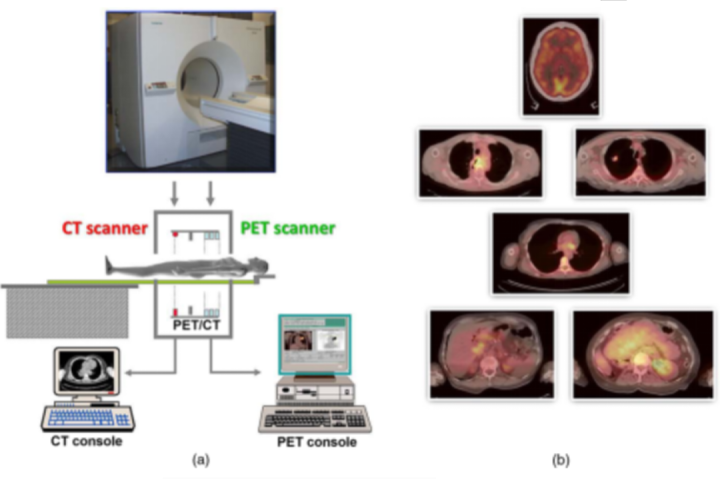
图14 第一台正电子发射断层扫描仪设计
(a) 将螺旋CT扫描仪与安装在与CT相同支架上的正电子发射断层扫描仪相结合。首先通过扫描仪连续移动床来获取CT图像,而后获取PET图像(b)
计算机断层扫描和正电子断层扫描的融合图像显示在屏幕上,供医师阅读。PET/CT扫描仪的广泛应用带来了许多其他的进步,从而提高了图像质量。包括呼吸和心脏门控,尤其是在胸部成像时。呼吸可以通过胸部周围的压力带或通过跟随放置在胸部上的标记的移动来进行外部监测。可以根据呼吸或心脏信号的多门电路进行连续采集。正电子发射断层扫描提供了使用4-D断层扫描来校正运动的可能性,尽管其代价是增加对患者的辐射剂量。减少x射线通量(从而减少辐射剂量)并使用迭代重建技术,可以用对患者较低的辐射剂量获得质量比较优良的图像。最后,西门子mCT上引入的创新是连续床运动采集,而不是全身成像的传统步进拍摄方法。它将全身作为一个单一的3-D体积,而不是多个单独的床位置。
大约20世纪90年代中期,在正电子断层扫描成为临床现实之前,临床前领域对正电子断层扫描和磁共振的结合产生了相当大的兴趣。这主要是因为磁共振与CT相比,可以获得更好的软组织对比度,在小动物成像时特别有用。然而,正电子断层扫描使用的光电探测器(光电倍增管)无法磁场中工作,需要屏蔽磁场。因而PET探测器与磁共振扫描仪协同操作较为困难。直到本世纪初,才开发出稳定、高效、低噪声、快速且在合理温度下工作的半导体光电探测器,2005年被用于临床前成像设备。2006年,西门子医疗保健分子成像公司生产了第一个使用可插入3T临床核磁共振仪中的光子晶体探测器环,以便在核磁共振仪运行的同时获取光子晶体数据。环的直径限制了对大脑的研究,该公司只生产了五个这样的插入物。在2010年,西门子在慕尼黑技术大学安装了第一台具有同步成像能力的正电子发射断层扫描/MR仪,该设计引起了极大的兴趣,随后的4年,全球安装了80台( 图15)
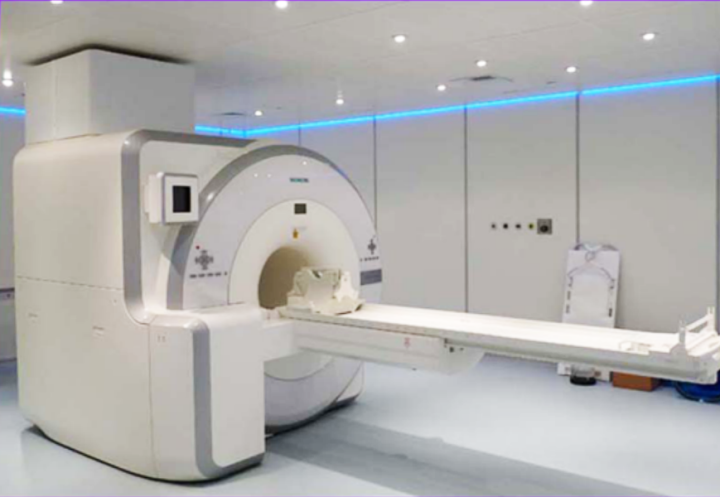
图15 第一台正电子/磁共振成像仪(西门子公司)
PET/MR的优点是软组织对比更好,无辐射剂量,对儿科患者和脑、肝、心脏和关节成像有明显的益处。同样在2010年,飞利浦推出了他们的PET/MR,将磁共振和PET分开,配备同一张床,将病人从磁共振转到PET;在3T磁共振扫描仪的3米范围内,需要额外屏蔽PET扫描仪,因此,该设计不允许同时对PET和MR成像。如前所述,同机设计的一个优点是,磁共振导航序列可用于监测运动并随后校正PET数据,而不会增加PET/CT上的四维CT采集中隐含的辐射剂量。这是正电子发射/磁共振的一个重要优点。PET/MR无疑将在临床上与PET/CT并列,起到越来越重要的作用。
上世纪70年代至今,正电子发射断层扫描仪的性能和复杂性都有了极大的提高,以ECAT II为例,它在1976年由66个探测器、363条响应线组成,点源灵敏度估计为0.16%。将这一性能与最先进的四环西门子生物描记器正电子发射断层扫描仪进行比较,该扫描仪包括448个探测器元件、136条响应线,测得的点源灵敏度为6.4%。因此,自加州大学洛杉矶分校实施ECAT II以来的40年中,灵敏度的提高了40倍,这是一项重大成就。
发展和展望
正电子发射断层成像,目前临床应用日益增多,具有很大应用潜力。自20世纪70年代以来,PET仪器的技术发展使图像质量有了很大提高。这些进步,被证明具有成本效益。物理学家、工程师和医学家(尤其是影像医学医生)联合起来面对这一重大技术挑战。推动正电子发射断层成像在临床研究和医疗保健中的应用。